La réponse à cette question clé repose sur un enseignement scientifique obsolète : les cours de sciences présentent un modèle erroné de l'eau liquide, perpétuant ainsi une méconnaissance généralisée.
Commençons par les bonnes nouvelles. Les modèles scientifiques de la molécule d'eau isolée, de la glace et de la vapeur d'eau sont corrects et servent de base solide. Reprenons-les avant d'aborder le problème central.

La molécule d'eau, pierre angulaire de toutes ses formes, associe deux atomes d'hydrogène à un atome d'oxygène 16 fois plus lourd. Électriquement neutre, elle est polaire : les centres des charges positives et négatives ne coïncident pas (Fig. 1). Les hydrogènes sont partiellement positifs, l'oxygène négatif. Cette forte polarité explique pourquoi l'eau, molécule légère, reste liquide à température ambiante.
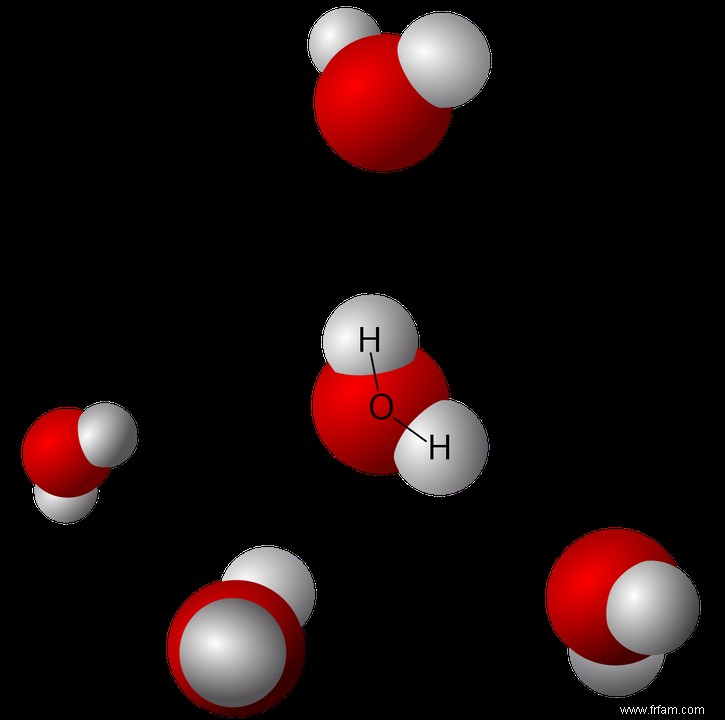
Les molécules polaires s'attirent via des liaisons hydrogène : hydrogènes positifs vers oxygènes négatifs (Fig. 2). Ces liaisons orientent les molécules et sont essentielles dans la glace, responsable de sa structure solide. Dans la vapeur, les molécules trop éloignées les ignorent.
La glace hexagonale relie chaque molécule à quatre voisines dans un réseau rigide (Fig. 3, gauche). Cela explique sa solidité et sa faible compressibilité.
La vapeur d'eau (Fig. 3, droite) montre des molécules espacées, mobiles et aléatoirement orientées : faible densité, haute compressibilité.
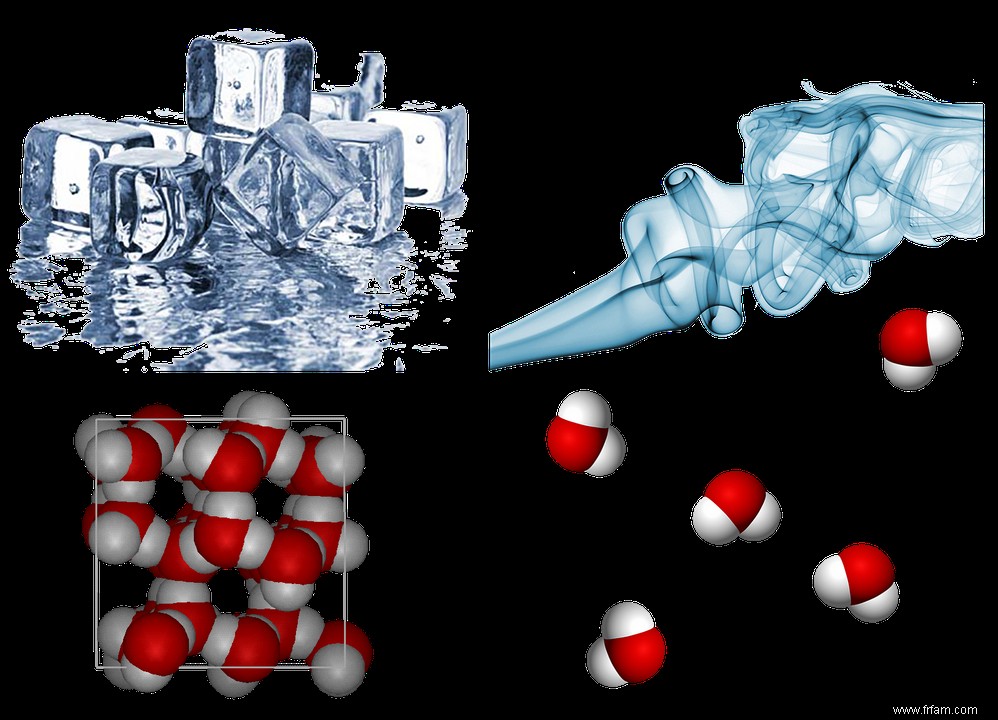
L'eau liquide pose problème : sa densité et compressibilité rappellent la glace, impliquant des molécules proches. Comment expliquer sa fluidité ?

Les manuels comparent souvent l'eau liquide à des "billes dans un sac" (Fig. 4), mobiles librement. Mais si les molécules sont proches, pourquoi ignorer les liaisons hydrogène ? Dans l'eau, plus dense que la glace, la polarité devrait primer. L'argument de l'énergie thermique (plus élevée en liquide) est faible : à 0°C, eau et glace coexistent avec la même énergie moléculaire.
Ce modèle "gazeux" simplifie à outrance, négligeant les interactions moléculaires pour expliquer la fluidité.
Des données confirment : chaleur de sublimation de la glace (51 kJ/mol) vs. fusion (6 kJ/mol). Seulement 12 % des liaisons hydrogène se rompent à la fusion. L'eau liquide conserve une structure liée, non un gaz.

La liquidité est une propriété de certains solides sur des échelles de temps humaines (ex. : poix coulante, glaciers comme "rivières fixes"). Voir Veritasium : "Is glass liquid?".
L'eau liquide est plus proche de la glace que de la vapeur : structure solide avec liaisons hydrogène partielles. Ce blog propose un modèle innovant, robuste, appuyé sur des études scientifiques. La version anglaise, avec références, est disponible via ce lien.