Ethan Bier est professeur de biologie cellulaire et du développement à l’Université de Californie à San Diego. Cet article a été initialement publié sur The Conversation.
Pourquoi les humains ressemblent-ils à des humains plutôt qu’à des chimpanzés ? Bien que nous partagions 99 % de notre ADN avec les chimpanzés, nos visages et nos corps diffèrent profondément.
La forme et l’apparence du corps humain ont évolué de manière significative, mais certains gènes contrôlant les caractéristiques distinctives des espèces sont restés étonnamment stables. En tant que biologiste spécialisé en évolution et développement, j’ai consacré de nombreuses années à étudier comment les gènes façonnent l’apparence des humains et des animaux.
Les récentes recherches de mon laboratoire éclairent le fonctionnement de ces gènes inchangés depuis des centaines de milliers d’années, expliquant comment ils modulent l’apparence des espèces au fil de l’évolution.
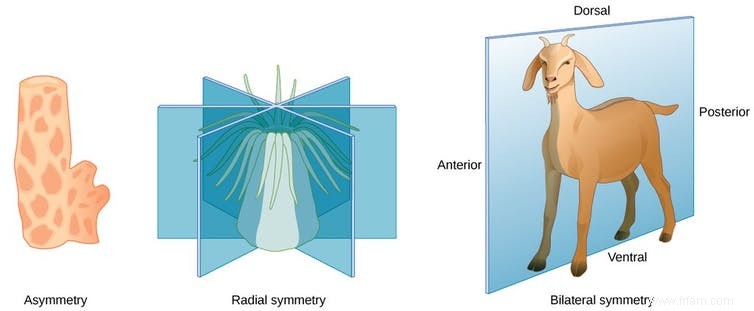
En biologie, le plan corporel décrit l’organisation d’un animal de la tête à la queue. Tous les animaux à symétrie bilatérale – dont les côtés gauche et droit sont miroirs – partagent des plans similaires : tête à l’avant, membres au milieu, queue à l’arrière.
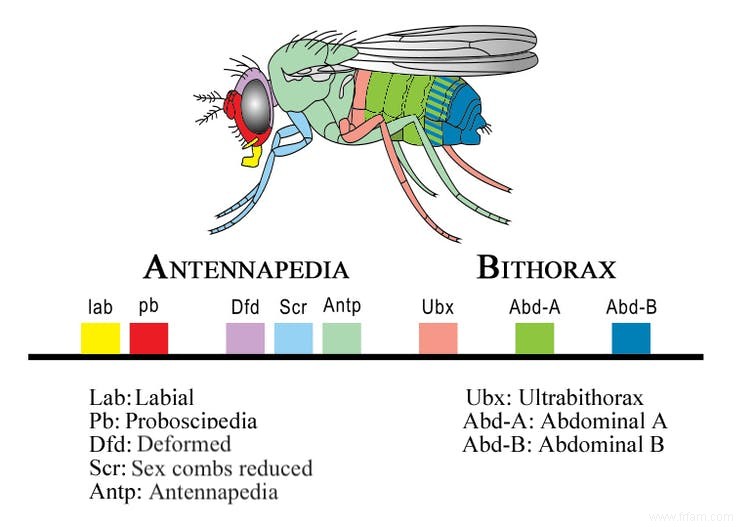
Les gènes Hox, sous-ensemble des gènes homéobox impliqués dans le développement anatomique, agissent comme un GPS génétique. Ils déterminent l’identité de chaque segment corporel, assurant que les membres émergent du torse et non de la tête, en régulant d’autres gènes responsables de structures spécifiques.
Tous les animaux possèdent des gènes Hox exprimés dans des régions similaires, et ces gènes sont conservationnés sur l’échelle évolutive. Comment restent-ils stables tout en étant cruciaux pour le développement ?
En 1990, le biologiste moléculaire William McGinnis s’est demandé si les gènes Hox d’une espèce fonctionnaient chez une autre. Actifs dans des zones comparables chez les mouches des fruits, humains ou souris, l’idée d’interchangeabilité semblait audacieuse.
Imaginez les pièces automobiles : rarement compatibles entre marques après un siècle. Pour mouches et mammifères, séparés par plus de 500 millions d’années, c’était inimaginable.
Cependant, insérer des gènes Hox de souris ou humains dans des mouches et les activer dans des zones inadaptées – comme un gène de jambe humaine à l’avant de la tête d’une mouche – a produit des antennes transformées en pattes. Les signaux positionnels humains restaient lisibles chez la mouche.
La question clé : comment ces gènes définissent-ils l’identité des régions corporelles ?
Deux hypothèses s’affrontent. L’hypothèse instructive voit les gènes Hox comme des « maîtres-régulateurs » dictant directement la forme des structures.
Celle de McGinnis propose un code positionnel : les gènes marquent des sites spécifiques, et l’évolution assigne des structures adaptatives à ces codes pour optimiser la survie – antennes chez la mouche, clavicules sous le cou chez l’humain.
Dans une étude récente publiée dans Science Advances, Ankush Auradkar, doctorant supervisé par un mentor de McGinnis et moi-même, a testé ces idées sur Drosophila melanogaster (D. mel).
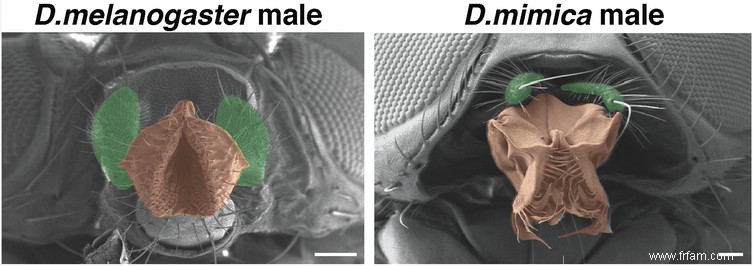
Auradkar a utilisé CRISPR pour remplacer le gène Hox proboscipedia (pb) de D. mel par celui de sa cousine hawaïenne Drosophila mimica (D. mim), qui contrôle des pièces buccales en forme de gril. Si instructive, D. mel développerait des grils ; si code positionnel, non.
Conformément à McGinnis, pas de grils, mais un trait D. mim émergea : les palpes maxillaires, saillants chez D. mel, s’alignèrent parallèlement à la bouche. Le gène pb fournit à la fois position et instructions partielles.
Auradkar a élucidé l’orientation des palpes : non par altération de la protéine, mais par modulation de l’activation du gène dans les régions concernées. Cela souligne la conservation de la protéine Hox.
Les gènes Hox s’affrontent aussi évolutivement : l’un domine, déterminant les traits finaux. De subtils changements d’interactions morphent le corps.
Que retenir pour l’humain ?
Ces travaux éclairent l’évolution des plans corporels et pourquoi humains et chimpanzés divergent.
Ils aident aussi à comprendre les malformations congénitales (fente labiale, cardiopathies), dues à des dysfonctionnements Hox. CRISPR pourrait offrir des thérapies pour ces troubles, comme la dystrophie musculaire.
 []
[]